ACIDOS CARBOXILICOS
Laboratorio química
- Objetivo: Identificar y conocer sobre las propiedades físicas y químicas de los ácidos carboxicos y sus usos

¿Qué son?
Los ácidos carboxilicos son compuestos orgánicos que tiene la presencia del grupo funcional carboxilo unido a un radical o una cadena hidrocarbonada. Su formula general es R-COOH ó R-CO2H, este consta de un atomo de carbono unido a un atomo de oxigeno mediante un enlace doble (C=O), y un grupo hidroxilo (-OH) por un enlace sencillo, R se puede referir a un grupo alquilo, alquenilo, arilo u otro. Los ácidos carboxílicos pueden ser saturados, insaturados o aromáticos.
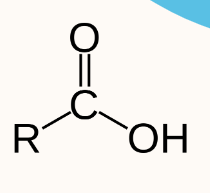
Propiedades físicas
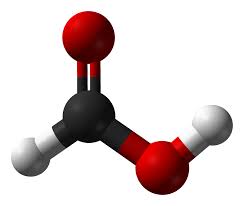
ESTADO FÍSICO: A temperaturas ambiente, los ácidos carboxílicos de cadena corta son líquidos, mientras que los de cadena larga son sólidos.
OLOR: Muchos ácidos carboxílicos tienen olores fuertes y distintivos. Por ejemplo, el ácido butanoico tiene un olor similar al de los quesos rancios.
SOLUBIDAD: Los ácidos carboxílicos de bajo peso molecular son solubles en agua, ya que pueden formar enlaces de hidrógeno con las moléculas de agua. A medida que aumenta el número de átomos de carbono, la solubilidad disminuye.
ACIDEZ: Son compuestos ácidos, lo que significa que pueden donar protones en solución, lo que les atribuye un pH menor a 7 en soluciones acuosas.
PUNTO DE EBULLICION: Los ácidos carboxílicos hierven a temperaturas aún más altas que los alcoholes. Estos puntos de ebullición tan elevados se deben a que un par de moléculas del ácido carboxílico se mantienen unidas por un doble puente de hidrógeno.
PUNTO DE FUSION: El punto de fusión varía según el número de carbonos, respectivamente. Después de 6 carbonos el punto de fusión se eleva de manera irregular. Esto se debe a que el aumento del número de átomos de carbono interfiere en la asociación entre las moléculas.
Propiedades químicas
ACIDEZ: Son ácidos débiles, lo que significa que pueden liberar protones (H⁺) en solución.
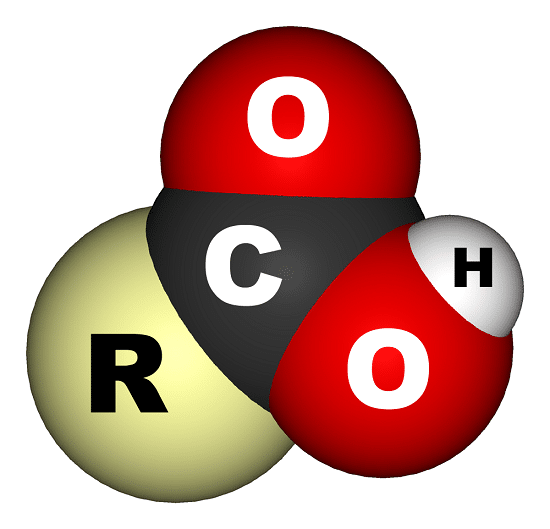
REACCIONES DE NEUTRALIZACION: Pueden reaccionar con bases para formar sales y agua
FORMACION DE AMIDAS: Al reaccionar con aminas, los ácidos carboxílicos pueden formar amidas, liberando agua. Se obtienen al reemplazar el grupo -OH del ácido carboxílico por el grupo -NH2.
OXIDACION: Son resistentes a la oxidación y a la reducción pero el hidruro de litio y aluminio los reduce hasta los alcoholes. implica transformaciones que pueden llevar a la formación de productos menos oxidados, como aldehídos o cetonas.
DECARBOXILACION: Algunos ácidos carboxílicos pueden perder dióxido de carbono (CO₂) al ser calentados o en presencia de ciertos reactivos. Son reacciones en las que el R−C enlace se rompe de tal manera queCO2se pierde y R−H se forma.